Esta regla nos dice que en un estado cuántico sólo puede haber un electrón. De aquí salen los valores del espín o giro de los electrones que es 1/2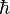 y con proyecciones
y con proyecciones  .
.
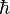 y con proyecciones
y con proyecciones  .
.También que en una orientación deben de caber dos electrones excepto cuando el número de electrones se ha acabado por lo cual el orden que debe de seguir este ordenamiento en cada nivel es primero los de espín positivo (+1/2) y luego los negativos.
El principio de exclusión de Pauli fue un principio cuántico enunciado por Wolfgang Ernst Pauli en 1925. Establece que no puede haber dos fermiones con todos sus números cuánticos idénticos (esto es, en el mismo estado cuántico de partícula individual). Perdió la categoría de principio, pues deriva de supuestos más generales: de hecho, es una consecuencia del teorema de la estadística del spin. El principio de exclusión de Pauli sólo se aplica a fermiones, esto es, partículas que forman estados cuánticos antisimétricos y que tienen espín semientero. Son fermiones, por ejemplo, los protones, los neutrones y los electrones, los tres tipos de partículas subatómicas que constituyen la materia ordinaria
No hay comentarios:
Publicar un comentario